Mais lidas 🔥

Inovação no campo
Nova variedade de banana chama atenção de produtores no ES

Rio Grande do Sul
Azeite brasileiro atinge nota máxima e é eleito o melhor do mundo em concurso na Suíça

Chuva de um lado, seca de outro
El Niño de 2026/2027 pode repetir a força e os impactos do fenômeno de 2015/2016?

Desenvolvimento rural
Mais de 161 mil mudas impulsionam produção no Norte do ES

Produção artesanal
Valença, no Rio de Janeiro, conquista 13 medalhas no Mundial do Queijo
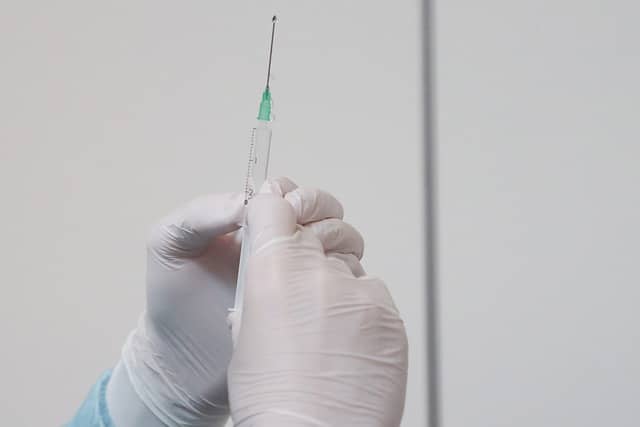
Um pedido de Autorização de Uso Emergencial para a versão da vacina bivalente contra a Covid-19, desenvolvida pelo laboratório farmacêutico Moderna e comercializada pela Adium, foi apresentado à Agência Nacional de Vigilância Sanitária (Anvisa).
Segundo a Anvisa, a vacina bivalente contém uma mistura de cepas do vírus SARS-Cov-2 e promete conferir maior proteção à variante Ômicron, quando comparada com vacinas monovalentes. Por sua transmissibilidade, observa a agência, a variante Ômicron causa preocupação às autoridades sanitárias do país.![]()
![]()
A Adium havia apresentado o pedido de registro da vacina, em janeiro. “Este pedido se encontra em análise pela equipe técnica da Anvisa. Porém, a empresa decidiu protocolar a Autorização de Uso Emergencial, paralelamente ao pedido do registro, de acordo com a manifestação favorável do Ministério da Saúde, conforme previsto no parágrafo único do Art. 1º da Resolução (RDC) 688, de 13 de maio de 2022”, explicou a agência, em nota.
Uso Emergencial
Uma vez recebido o pedido de Autorização de Uso Emergencial, a Anvisa tem 30 dias para concluir sua avaliação. Esse prazo é interrompido sempre que for necessário solicitar à empresa a complementação de informações ou esclarecimentos sobre os dados de qualidade, de eficácia e de segurança apresentados.